¿Estudias física y necesitas dominar este tema rápido? En esta guía encontrarás cada ley explicada de forma clara y sencilla, con ejemplos visuales que te ayudarán a recordarlas fácilmente para tu examen.
En este artículo te explicaremos cuáles son las 4 leyes de la termodinámica (o los principios de la termodinámica). También te mostraremos algunos ejemplos en como se aplica a nuestro diario vivir.
La termodinámica es una rama de la física que se encarga de estudiar las transformaciones de la energía en relación con el calor y el trabajo mecánico. El significado de termodinámica deriva del griego thermo que significa «calor» y dynamis que significa «potencia».
¿Qué son las leyes de la termodinámica?
La termodinámica establece cuatro leyes fundamentales: el equilibrio termodinámico (o ley cero), el principio de conservación de la energía (primera ley), el aumento temporal de la entropía (segunda ley) y la imposibilidad del cero absoluto (tercera ley). Las leyes de la termodinámica estudian y describen los sistemas termodinámicos y como interactúan con su entorno.
Un sistema termodinámico es una parte del universo (conjunto de materia) que se aísla (de manera real o teóricamente) para poder estudiarla. Así hay tres tipos de sistemas, los sistemas abiertos, que se dan cuando hay un intercambio de energía y materia con el entorno. Los sistemas cerrados son donde no hay intercambio de masa pero si de energía con el exterior. Y, los sistemas aislados son en los que no hay transferencia de energía y materia con los alrededores.
Las cuatro leyes o principios de la termodinámica describen como se comportan la energía, temperatura, y la entropía en los sistemas termodinámicos (moléculas, personas, planetas). También establecen ciertos límites en como se intercambia y transforma la energía en los procesos termodinámicos y explica el porqué es imposible construir una máquina de movimiento perpetuo.
Cada ley se formuló en diferentes épocas y se establecieron en diferentes órdenes. Curiosamente se formularon primero la primera, segunda y tercera ley de la termodinámica. Luego se formuló una última ley, pero, se percataron que por orden y concepto debía ir primero que todas. Así, esta se llamó la ley cero de la termodinámica.
Algunas de sus aplicaciones las podemos ver, cuando prendemos un aire acondicionado cuando hace mucho calor, o por otro lado, cuando necesitamos preservar nuestros alimentos dentro de los refrigeradores o neveras.
Ley cero de la termodinámica: equilibrio térmico
Llamada también ley de equilibrio térmico o a veces ley de igualación de temperaturas. Entre las leyes de la termodinámica, esta fue la última en consolidarse. Fue propuesta en 1930 por Guggenheim y Fowler.
Si tenemos un objeto A en equilibrio térmico con un objeto B, y este último también está en equilibrio con otro objeto C, entonces A y C también estarán en equilibrio térmico. Es decir: si A = B y B = C, entonces se tiene que A= C.
Básicamente se refiere a que si dos objetos A y B están en contacto térmico a diferentes temperaturas, entonces se producirá una transferencia de calor, y si colocamos un tercer objeto C (como un termómetro) con cualquiera de estos objetos mencionados, entonces con el tiempo todos llegarán a un equilibrio térmico (igualación de temperaturas). Este es el principio físico de un termómetro, el cual usamos para medir la temperatura al ponerlo en contacto con otro cuerpo.
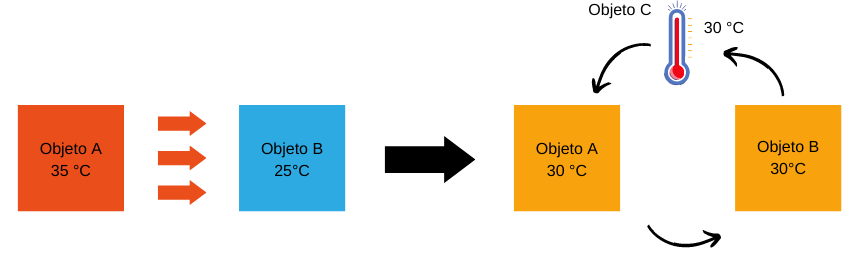
También con la ley cero se puede definir lo qué es temperatura. Así la temperatura en termodinámica es una medida de la energía interna de un cuerpo, es decir la energía cinética producto del movimiento de las moléculas. En nuestro día a día se relaciona con nuestra sensación térmica, donde un cuerpo «caliente» tiene más temperatura que uno «frío» (aunque eso no siempre es así).
Ejemplos de la ley cero
- En los termómetros: al colocarlo en nuestra piel, nuestro organismo entrará en equilibrio térmico con el vidrio del termómetro, y este último con el mercurio (Hg). Todas las temperaturas estarán igualadas, por ende, sabremos la magnitud de la temperatura de nuestro cuerpo.
- En un refrigerador: si colocamos unos envases de diferentes temperaturas dentro del compartimiento donde la temperatura está a 3 °C, entonces, al pasar el tiempo todos envases alcanzarán dicha temperatura.
- En una hielera: si colocamos un café y un jugo de naranja adentro de la hielera, después de unos minutos todos tendrán la misma temperatura (equilibrio térmico).
Primera ley de la termodinámica: principio de conservación de energía
La primera ley de la termodinámica describe la relación entre el intercambio de calor, energía interna y trabajo de un sistema termodinámico. Es una extensión del principio de conservación de energía. Fue propuesta en 1860 por Rudolf Clausius y William Thompson (Lord Kelvin) basándose en los trabajos de Sadi Carnot.
El primer principio de la termodinámica puede estar expresado de muchas maneras, aquí la definimos así:
![]()
El cambio de la energía interna de un sistema cerrado es igual al calor suministrado al sistema menos el trabajo realizado por el sistema.
Equivalentemente, podemos escribir:
![]()
En todo proceso termodinámico, la cantidad de calor (Q) que el sistema recibe o pierde se utiliza en parte para realizar trabajo externo (W) y el resto se absorbe para aumentar o disminuir la energía interna (U) del sistema.
Podemos explicarlo de la siguiente manera: si en un sistema hay un aumento de energía, no significa que se haya creado energía. De igual modo, cuando disminuye la energía, no se destruye; simplemente se transforma en otro tipo de energía. Es decir, la energía se conserva.
Así, el calor intercambiado con el entorno corresponde a la diferencia entre el cambio de energía interna del sistema y el trabajo que realiza. La energía no puede crearse ni destruirse, solo transformarse de una forma a otra, permaneciendo constante. Por ejemplo, la energía química de un combustible puede convertirse en energía mecánica para mover una aeronave, pero la cantidad total de energía se conserva, tal como establece la primera ley de la termodinámica.
Energía interna de un sistema
Aquí, se introduce el concepto de energía interna. La cual es la suma de la energía de las partículas microscópicas que componen un sistema. La energía interna solo incluye la energía cinética y energía potencial que cada partícula tiene, más no la que surge de la interacción entre el sistema y su entorno.
En un proceso termodinámico
- Figura A, la energía interna (U) de un sistema aumenta si se agrega calor más que trabajo efectuado por este.
- En la figura B, la energía interna disminuye si en el sistema sale más calor que el trabajo efectuado.
- Figura C, la energía interna no cambia si el calor agregado es igual al trabajo que el sistema realiza.
Imagen 2: Foto: Sears-Zemansky
Es importar acotar la convención de signos:
- Calor positivo (+Q): cuando el sistema absorbe calor.
- Calor negativo (-Q): el sistema cede calor.
- Trabajo positivo (+W): cuando el sistema realiza trabajo sobre su alrededor.
- Trabajo negativo (-W): se da cuando se realiza trabajo sobre el sistema.

Ejemplos de la primera ley de la termodinámica
- Batir un chocolate frío: al batirlo le transferimos energía, lo cual también genera calor, por lo que su energía interna aumenta. (La energía fue transferida del batidor al chocolate. El chocolate no la creó).
- El motor de un carro: la energía se transforma de energía química a energía mecánica. La gasolina o diesel entra en reacción con el oxígeno (O2) generando una combustión y liberando calor, y es precisamente este calor que genera el movimiento de los pistones y cigüeñal. Así, si hacemos el cálculo de la gasolina consumida, el trabajo realizado y la cantidad de calor que expulsó el motor, obtendríamos que la energía total es constante.
- Gas en el interior de una botella: si dejamos una botella que contiene gas bajo el sol por un largo tiempo, es probable que explote. La energía del sol se transmite al gas aumentando su energía interna, provocando que este se expanda (realice trabajo) y provoque el estallido.
Segundo principio de la termodinámica o Ley de la Entropía: la dirección de los procesos termodinámicos
Esta es quizás la más famosa de las cuatro leyes de la termodinámica. Establece límites en la transformación o uso de la energía y la dirección en que los procesos termodinámicos pueden ocurrir. Fue propuesta por Nicolás Léonard Sadi Carnot en 1824 (esta ley fue considerada anteriormente como la primera).
Límites en el uso de la energía
La segunda ley de la termodinámica nos dice que:
Es imposible que un sistema termodinámico efectúe un proceso en el que absorba todo el calor de una fuente caliente y lo convierta totalmente (100%) en trabajo mecánico, sin expulsar calor al exterior y que termine en el mismo estado en que inició.
En otras palabras, no hay manera que podamos construir un motor o dispositivo que convierta toda la energía calorífica en trabajo mecánico (no podemos obtener un 100% de eficiencia, siempre habrá pérdida de energía).

Dirección de los procesos termodinámicos
¿Alguna vez te has preguntado por qué cuando colocamos un objeto caliente como el café comienza a enfriarse y otro frío como unos cubos de hielo se calientan hasta derretirse? ¿Por qué no ocurre lo inverso? ¿Por qué el café no se calienta solo y los cubos de hielos no se siguen enfriando solos?
La experiencia nos dice que el calor se trasfiere del cuerpo más caliente al más frío. Pero, la primera ley de la termodinámica no establece un orden en la dirección de los procesos termodinámicos.
Bien, podría decirse que el calor del ambiente que tiene menor temperatura se transfiere al vaso de café que tiene mayor temperatura. Si esto fuera posible, no violaría la primera ley de la termodinámica, sin embargo esto no sucede en la vida real. En este caso el calor del café se transfiere al exterior, hasta que llegue a temperatura ambiente con el mismo (equilibrio térmico).
Con respecto a los cubos de hielos, se derretirán porque ganan calor del ambiente o de un cuerpo más caliente que ellos. En la naturaleza no hay un proceso, donde de manera natural el calor fluya desde lo más frío a lo más caliente. Esto no ocurre al menos que se emplee ingeniería para mantener la temperatura. Como por ejemplo, en los refrigeradores o neveras. Así, la segunda ley de la termodinámica establece un orden en la dirección de los procesos termodinámicos.
Relación del segundo principio de la termodinámica y la entropía
Por otro lado, también podemos ver la segunda ley de la termodinámica de acuerdo a un término importante, la entropía.
La entropía se podría definir de manera macroscópica como: una medida cuantitativa del grado desorden de un sistema. Y, en una perspectiva microscópica como: una medida de las probabilidades de las diferentes configuraciones de los estados en un sistema, es decir: indica que «evento» es más probable que ocurra.
La entropía determina la dirección del propio tiempo. Es la “flecha del tiempo” que establece el flujo de los sucesos hacia adelante y permite distinguir los sucesos pasados de los futuros. En otras palabras la entropía describe lo reversible e irreversible de los sistemas termodinámicos. Todos los sistemas naturalmente tienden a desequilibrarse con el tiempo, es decir la entropía siempre aumenta y por ende, también la entropía del universo.
Así, si quemas un libro, nunca volverá a ser igual, porque parte de él está en las cenizas y otra se fue al ambiente en forma de calor y CO2, aumentado así la entropía del lugar y el universo.
Por eso, también, es más probable que se enfríe un té, a que este se caliente por su propia cuenta. De igual manera, si se rompe una taza, esta ya no se podrá reparar para que quede perfectamente igual que antes.

De interés:
¿Qué son los agujeros negros? Todo lo que debes saber
Tercera ley de la termodinámica: Ley cero absoluto
El cero absoluto (0 K, igual a -273,15 °C) es la menor temperatura, que en teoría la materia podría existir. Experimentalmente, es imposible llegar a esta medida, así como también, es imposible construir una máquina que sea de movimiento perpetuo.
Si pudiéramos hacer que un objeto llegara al cero absoluto sus átomos se detendrían (según la física clásica), pero según la mecánica cuántica, siempre se requiere un tipo de movimiento para no violar el principio de incertidumbre de Heisenberg.
Al aproximarse al cero absoluto, se producen fenómenos interesantes en la materia como por ejemplo:
- Superfluidez: elementos como el helio (He) se transforman en un líquido casi sin viscosidad.
- Superconductividad: la electricidad se conduce casi que sin resistencia. Mucho mejor que en el cobre (Cu) o el oro (Au).
La ley cero absoluto fue postulada por Walther Hermann Nernst
Indica:
Es imposible que un objeto o sustancia pueda llegar al 0 absoluto a través de un número de procesos finitos, donde su entropía sea mínima. Nos podemos acercar a esa medida, pero no alcanzarla.

Aplicaciones de la ley del cero absoluto
Los científicos se han acercado mucho, en 2014 enfriaron cobre de un volumen de un metro cúbico a 0,006 Kelvins (-273.144 °C) durante 15 días, estableciendo un récord para la temperatura más baja registrada en el universo conocido sobre un volumen tan grande.
Algunas aplicaciones del cero absoluto:
- Aceleradores de partículas como en el LHC del CERN.
- Levitación magnética: trenes bala.

Resumen y conclusión de las leyes de la termodinámica
Con lo que vimos, podemos indicar que estas 4 leyes de la termodinámica rigen todo lo relacionado con la temperatura, trasferencia de calor y estados de la materia. Tienen una gran aplicabilidad en el mundo que nos rodea, está en las neveras, motores, aires acondicionados, en el universo.
De las leyes de la termodinámica se pueden mencionar cosas muy importantes como que, la ley del cero absoluto de la termodinámica, es la base utilizada en la física e ingeniería de un termómetro. Por otro lado, la primera ley permite la trasformación de energía en los sistemas. Pero, no coloca un límite y direccionalidad de los procesos que ocurren en la naturaleza, por ejemplo, nunca vemos una pelota acumular energía potencial (energía interna) y comenzar a dar saltos por su propia cuenta.
Sin embargo, con la segunda ley de la termodinámica, si nos coloca una restricción en el orden de los hechos, es por eso que, una bola de tenis que se arroja al piso, rebotará hasta que llegue al reposo (el proceso natural). De igual manera, es importante saber que, el calor siempre fluye de manera natural desde el cuerpo o fuente de mayor temperatura al de menor temperatura.
Por otro lado, la tercera ley nos coloca una restricción, en la que no podemos llegar al 0 K (cero absoluto) mediante muchos procesos termodinámicos. Pero al intentar esto, hemos encontrado maravillosas aplicaciones con estados de la materia que nunca habíamos visto, como la superconductividad, superfluidez.
Te dejamos estos dos videos donde se explican de manera similar las 4 leyes de la termodinámica para que relaciones conceptos.
Bibliografía
Flores, C., Ramos, E. y Rosales, N. (2010). Ciencias o filosofías de la naturaleza. Panamá: Imprenta Articsa.
Hugh, Y y Freddman, R. (2009). Física Universitaria. México: Pearson Educación.





Pingback: REVENIDO TERMOQUÍMICO: Diagrama de Fases – Cidepa
Este artículo me parece espectacular
Gracias amigo !!!
¡Qué bueno que te haya gustado el artículo Luciano!:D